No es el primer paciente que me pregunta si no existe algún suplemento nutricional eficaz para perder peso, inclusive en la primera consulta, es decir antes de haber iniciado la dieta. Resulta llamativo, que a priori la persona ya esté aferrándose a una ayuda extra que promueva la pérdida de peso, sin haberse adherido aunque sea mínimamente a aquella.
El tratamiento de la obesidad es un mercado que genera un gran beneficio económico. Esto explica que existan muchos intereses comerciales y un fuerte marketing nutricional alrededor del ámbito de la suplementación antiobesidad. Si estás familiarizado con las dietas orientadas a la pérdida de peso seguro que te resultan conocidos nombres como Camelia sinensis, citrus aurantium, chitosan, Garcinia Cambogia (GC)... Todos ellos son suplementos basados en extractos de plantas.
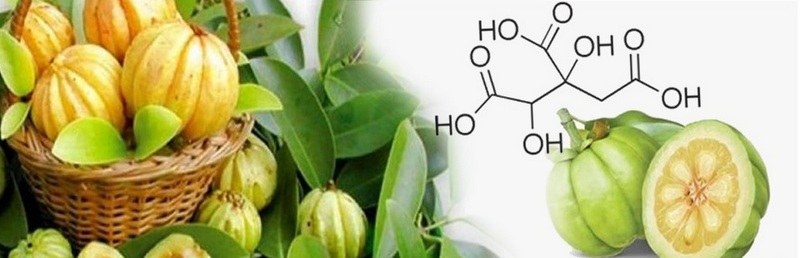
En esta ocasión se resume el interesante artículo de Crescioli G y Col (2) donde describen cuatro casos clínicos sobre el efecto hepatotóxico de la GC y realizan una revisión de estudios de la literatura sobre dicho tema.
Indice
3-Efectos tiene el HCA sobre la regulación del peso y el gasto energético.
4-Mecanismo de acción del HCA.
5-Eficacia de la GC para bajar de peso.
8-Serie de casos descritos por Crescioli G y Col.
Es una planta cuyo principio activo (aquel al que se le atribuye un efecto antiobesidad) es el Ácido Hidroxicítrico (HCA) (1,2).
El compuesto bioactivo es el Ácido Hidroxicítrico (HCA), molécula que guarda analogía estructural con el ácido cítrico (1,2).
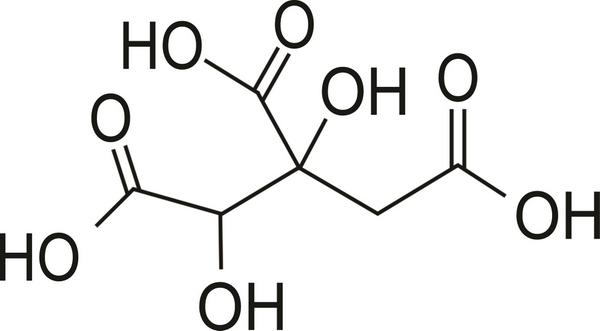
3-Efectos tiene el HCA sobre la regulación del peso y el gasto energético.
En modelos animales tiene un efecto anorexígeno (inhibe la ingesta alimentaria) y reduce la lipogénesis (formación de tejido adiposo) (1,2).
4-Mecanismo de acción del HCA.
El HCA inhibe la liasa del ácido cítrico, enzima que media en la síntesis de ácidos grasos (1,2).
5-Eficacia de la GC para bajar de peso.
Aunque en modelos animales reduce el apetito y el peso corporal la mayor parte de estudios en seres humanos fallan al tratar de replicar dichos hallazgos. Además la magnitud del efecto es pequeña y los resultados no son reproducibles (2).
6-Seguridad de la Garcinia Cambogia.
Una de las principales preocupaciones son los aspectos de seguridad, debido a su efecto hepatotóxico (1,2).
7-Criterios de búsqueda de estudios sobre la eficacia de la mesoterapia en el sobrepeso, obesidad y alteraciones estéticas asociadas (celulitis, piel de naranja…).
Si imponemos una búsqueda de artículos con las siguientes condiciones: inclusión del término “Garcinia Cambogia” en el título y la presencia de “hepatotoxicity” y/o “liver failure” y/o “hepatitis”: “Garcinia Cambogia” [title] AND (“hepatotoxicity [title]” OR “liver failure” [title] OR “hepatitis” [title]) el buscador devuelve 6 artículos. Sin embargo la revisión de Crescioli G y Col alude a otros muchos estudios que cuestionan seriamente la seguridad de GC.
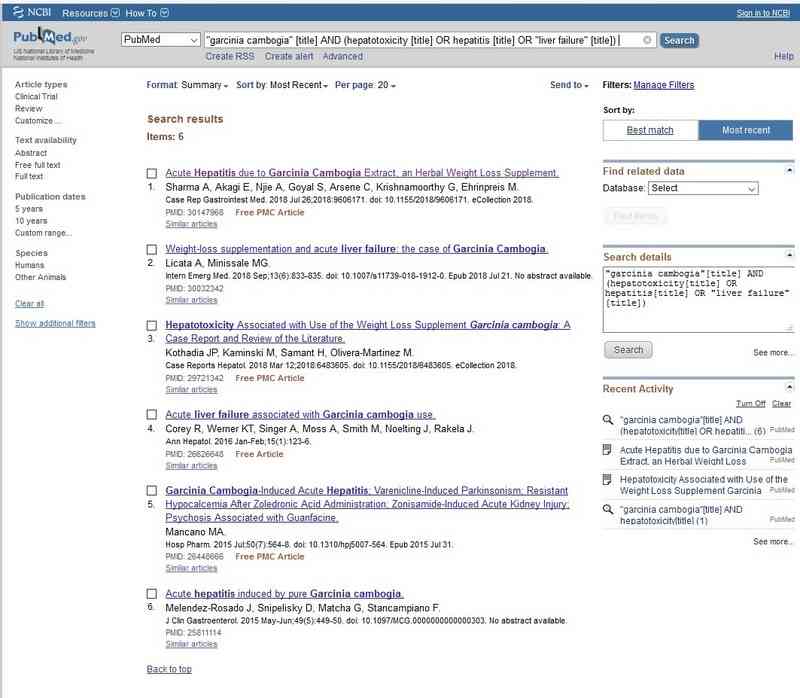
8-Serie de casos descritos por Crescioli G y Col.
Crescioli G y Col que describieron cuatro casos clínicos relacionados con el daño hepatotóxico de GC.
Mujer de 61 años que acudió a Urgencias con síntomas de dolor abdominal de 10 días de duración, náuseas, debilidad progresiva, ictericia, orina oscura y heces de tonalidad pálida. La mujer refiere antecedentes personales de colecistectomía (extirpación de la vesícula biliar), dislipidemia mixta e hipotiroidismo a tratamiento con levotiroxina y ausencia de historia de alcoholismo y exposición a fármacos hepatotóxicos.
La paciente refirió llevar tomando un sobre/día de un suplemento nutricional a base de extractos de plantas que contenía: GC (HCA 60%), Ananas comosus (bromelaína, 334 GDU -Unidades Disolventes de Gelatina-) y Ilex paraguariensis (2% cafeína).
La analítica en el momento de ingreso en Urgencias revelaba niveles elevados de ALT, AST, GGT, Billirubina Total (TB) y Fosfatasa Alcalina (ALP)
Tres meses antes la analítica era normal y se había descartado hepatítis vírica, Enfermedad de Wilson. Además la Ultrasonografía Abdominal (AU), la Colangiopancreatografía por Resonancia Magnética (MRCP) y la Ecografía Doppler eran normales lo que descartó una esteatosis hepática. Una Tomografía Computerizada (TAC) abdominal reveló un derrame peritoneal y linfadenopatía perihepática. Una biopsia hepática contribuyó al diagnóstico: hepatitis colestática. El aumento progresivo de TB remitió tras dos sesiones de plasmaféresis.
Al cabo de 4 semanas de suspender la ingesta del suplemento los síntomas remitieron y los parámetros de función hepática mejoraron paulatinamente. La paciente fue dada de alta sin precisar un transplante hepático. Al cabo de cuatro meses del ingreso en Urgencias los parámetros de daño hepatotóxico se habían normalizado.
Mujer de 39 que acudió a Urgencias con síntomas de astenia, pérdida de apetito ictericia y dolor en el hipocondrio derecho. La anamnesis reporta obesidad mórbida (BMI=44,9), HBP y hernia de hiato. La paciente refiere consumir tres fármacos: metildopa, domperidona y omeprazol y dos suplementos nutricionales para bajar de peso prescritos por su nutricionista (una marca comercial y una fórmula magistral):
El primero contenía 140 mg de extracto de C. aurantium al 10% (14 mg de sinefrina), GC (72 mg de HCA) Orthosiphon stamineus (0,2 mg de sinensetina) y Grifonia
simplicifolia (75 mg de 5-hidroxi-L-triptófano) por cápsula. Llevaba consumiendo 1 cápsula/día durante el último mes.
El segundo vehiculizaba 350 mg de extracto de C. aurantium al 6% (21 mg de sinefrina), 150 mg de Rhodiola rosea y 200 mg de extracto de O. stamineus por cápsula. Declara llevar consumiendo 1 cápsula/día durante la última quincena.
La analítica en el momento de ingreso en Urgencias revelaba niveles elevados de ALT, AST, GGT, TB, bilirrubina directa, ALP, LDH, PCR y MCV. Se descartó una hepatitis vírica, e infecciones víricas por citomegalovirus y virus varicela-zoster. Sin embargo los anticuerpos antinucleares no específicos y biliares fueron positivos. La AU fue normal. No se realizó una biopsia hepática.
Durante la hospitalización se suspendió el consumo de los fármacos y suplementos mencionados y la TB remitió gradualmente. Los síntomas y pruebas de función hepática también se normalizaron. Al cabo de 12 días de hospitalización la mujer fue dada de alta estableciéndose un diagnóstico de hepatitis colestásica aguda.
En relación a la etiología del cuadro se contempló la posibilidad de una hepatotoxicidad por ingesta simultanea de metildopa, altas dosis de sinefrina y HCA. Sin embargo los médicos refirieron que la causa más probable fuese una Lesión Hepática Inducida por
Plantas o HILI (Herb Induced Liver Injury).
Mujer de 47 años que ingresa en Urgencias con síntomas de dolor abdominal severo en el hipocondrio derecho. La anamnesis reporta HBP, hipotiroidismo y obesidad leve. La paciente refiere consumir dos fármacos: enalapril y levotiroxina y un suplemento antiobesidad que contiene cromo y 400 mg de extracto de GC al 50% (200mg de HCA) por cápsula. La mujer señala que lleva consumiendo 2 cápsula/día del mismo durante el último mes. La analítica en el momento de ingreso en Urgencias revelaba niveles elevados de ALT, AST y TB, principales marcadores de daño hepático. Se descartó hepatitis víricas y ausencia de autoanticuerpos. No se hallaron evidencias de esteatosis hepática. No se realizó una biopsia hepática.
Durante la hospitalización se suspendió el consumo del suplemento nutricional y la TB remitió gradualmente. Los síntomas y pruebas de función hepática también se normalizaron. El diagnóstico más probable fue HILI.
Mujer de 52 años que ingresa en Urgencias con un cuadro de hepatitis aguda. No se reportan antecedentes de enfermedades y tratamientos farmacológicos de interés. La paciente únicamente refiere consumir un suplemento para bajar de peso que contiene 400 mg de extracto de GC al 6% (240mg de HCA) y 400 mg de extracto de café verde al 50% (200 mg de ácido clorogénico) por cápsula. La paciente refiere que adquirió dicho producto a través de un anuncio televisivo y que llevaba consumiéndolo 1 mes.
La analítica en el momento de ingreso en Urgencias revelaba niveles elevados de ALT, AST, GGT, TB y ALP. Se descartó hepatitis víricas y ausencia de autoanticuerpos. No se hallaron evidencias de esteatosis hepática. No se realizó una biopsia hepática.
Durante la hospitalización se suspendió el consumo del suplemento nutricional y los valores se normalizaron paulatinamente. Los síntomas y pruebas de función hepática también se normalizaron. El diagnóstico más probable fue HILI
Cabe señalar que los autores en su revisión identificaron 32 estudios: 24 estudios de un caso y 8 de series de casos en un total de 66 pacientes después del consumo de extracto de GC.
En 17 estudios (53% de la muestra) con un total de 50 pacientes se asoció con un cuadro de lesión hepática, fallo hepático y hepatotoxicidad (3-19).
En 5 estudios (16%) episodios de manía y múltiples síntomas psicóticos (20-24).
En 5 estudios (16%) se reportaban miocarditis, cardiomiopatía, toxicidad por serotonina, hipoglucemia y trombocitopenia (25-29).
En 3 estudios (9%) rabdomiolisis (30-32).
En 2 estudios (6%) se refería pancreatitis y cetoacidosis diabética (33,34).
En 2 estudios (6%) el desenlace final fue la muerte. En el primer caso una mujer de 45 años que llevaba con un tratamiento de montelukast para el asma durante 5 años desarrolló un fallo hepático progresivo y rápido tras 7 días consumiendo dos suplementos dietéticos que contenían GC y C. Aurantium simultáneamente. Los autores postularon que el HCA aumentaba la toxicidad hepática del montelukast (3). En el segundo caso falleció a consecuencia de complicaciones de un transplante hepático (7).
El 62% de los pacientes eran mujeres sin un historial médico relevante. Todos los pacientes siguieron las indicaciones del fabricante y desarrollaron efectos adversos semejantes. Los valores alterados en suero sugestivos de daño hepático eran semejantes entre los afectados. Los efectos adversos más habituales fueron debilidad generalizada, ictericia, dolor abdominal, náuseas y vómitos. El tiempo de exposición al compuesto, debut, curso y desenlaces clínicos difirieron entre pacientes. Algunos llevaban consumiendo el suplemento días o semanas, otros mas de un año, 38 mejoraron y 8 precisaron un transplante hepático, un paciente fue diagnosticado con cirrosis hepática y 2 fallecieron.
No se ha descrito el mecanismo de toxicidad hepática exacto del HCA. Algunos estudios apuntan que promueve una deposición de colágeno hepático, peroxidación lipídica, aumento de la expresión de genes relacionados con la inflamación y estrés oxidativo, necrosis y apoptosis de los hepatocitos, fenómenos que subyacen a la hepatotoxicidad (2).
1-Se han descrito en la literatura biomédica varios casos de HILI (2).
2-Los suplementos con extracto de Garcinia Cambogia (GC) aislado o que lo incorporan simultáneamente en la misma matriz con otros ingredientes son uno de los más populares en el campo de la pérdida de peso (2).
3-Crescioli G y Col implementaron una revisión sobre los efectos adversos del consumo de GC, describieron cuatro casos clínicos que ponen de manifiesto su efecto hepatotóxico, e identificaron 32 estudios en una revisión de la literatura (2).
4-Los estudios mencionados sugieren una relación causal entre el consumo de GC y el desarrollo de una lesión hepática aguda. Esta aseveración es sustentada por el hecho de que los síntomas remiten cuando se suspende la ingesta del suplemento (2).
5-Dado que la mayoría de los suplementos contienen una mezcla de ingredientes es difícil atribuir el efecto a uno en particular (2).
6-Aunque existen suplementos nutricionales antiobesidad que se comercializan en Farmacias, Parafarmacias y tiendas de dietética, ninguno ha demostrado de forma robusta ser eficaz en seres humanos (1,2).
7-El consumo de algunos suplementos nutricionales puede conllevar efectos adversos de gravedad variable, sobre todo hepatotoxicidad, caso de la Garcinia Cambogia descrito más arriba (1,2).
8-El riesgo aumenta si la persona se autoprescribe el suplemento o recurre a lo que ha escuchado en su círculo de amistades, entorno de trabajo, gimnasio…
9-La regulación de la fabricación, venta y distribución de suplementos nutricionales no están sometidos a una normativa tan exigente como los fármacos, que precisan ser sometidos a ensayos clínicos antes de su lanzamiento al mercado y sólo pueden ser distribuidos en farmacias, la mayoría bajo prescripción médica. Como consecuencia no existe un balance riesgo-beneficio que permita asegurar la máxima latina “primum non nocere” (primero, no hacer daño) (35).

Por un lado puede ocurrir que dos lotes de un mismo producto de una marca determinada difieran en los ingredientes y/o concentraciones de las sustancias que vehiculizan.
Por otro lado puede suceder que estén contaminados con otras sustancias (pesticidas, micotoxinas, esteroides anabolizantes…)
Muchas de las alegaciones de los suplementos nutricionales están desprovistas de fundamento científico o no han sido adecuadamente regulados (35).
Estos comentarios no pretenden hacer apología de los alimentos y demonizar los suplementos nutricionales, sino enfatizar el vacío regulatorio de los segundos.
Si tenemos en cuenta que sólo existen tres fármacos aprobados en el tratamiento de la obesidad (bajo receta médica) en Europa (orlistat, liraglutide y naltrexona+bupoprión) y cuatro en EEUU (anteriores y topiramato+fentermina) (36) y como indicaba anteriormente el proceso que debe seguirse para comercializar un fármaco requiere una infraestructura compleja, dinero y mucha ciencia de calidad, resulta sorprendente la variedad de suplementos que se comercializan para perder peso.
10-Un argumento muy atractivo para el consumidor es la etiqueta “natural”. Se identifica erróneamente que todo lo natural es inocuo (e.g. la aflatoxina, una micotoxina producida por los hongos de la familia Aspergillus es natural, pero letal y la carne mechada que se comercializó sobre todo en Sevilla es natural, pero estaba contaminada con Listeria monocytogenes y en algunos casos fue letal). Pajor EM y Col hallaron que las consumidores y no consumidores atribuyen los efectos adversos a las características y/o comportamiento del sujeto (presencia de enfermedad, uso excesivo…) y no a la seguridad del suplemento nutricional (37).
11-No existe suplemento nutricional ni fármaco antiobesidad más eficaz que las dieta hipocalórica y el ejercicio aeróbico y de fuerza.
12-Desconfía de la información que puedas encontrar en Internet, sobre todo si al final de la lectura del artículo te propone la compra de un determinado suplemento y/o procede de personas que no sean profesionales o pseudoprofesionales. No juegues con la salud, pues es lo más preciado que tenemos. Si optas por tomar un suplemento nutricional consulta a un Dietista-Nutricionista.
13-Los profesionales biosanitarios, particularmente los Dietistas-Nutricionistas deberían prestar especial atención a las mujeres, por estar más preocupadas con su imagen y peso corporal, erigiéndose como un grupo de riesgo ya que con frecuencia recurren suplementos nutricionales para el control de aquel.
14-La investigación en el ámbito de la suplementación nutricional antiobesidad es un campo prometedor, aunque se precisa investigación de alta calidad tanto básica (para dilucidar los mecanismos moleculares) como de intervención en seres humanos, con un adecuado control de factores de confusión (otros alimentos, actividad física…)
15-Los alimentos son matrices complejas en las que los nutrientes y compuestos interaccionan entre sí. Un suplemento nutricional difícilmente podrá mimetizar el comportamiento metabólico de un alimento. Por esta razón creo que los alimentos funcionales (aquellos a los que se incorporan ingredientes que ejercen un efecto protector frente a la enfermedad o promueven el rendimiento deportivo…) constituyen un mejor abordaje a efectos de biodisponibilidad que los suplementos nutricionales.
1. Semwal RB, Semwal DK, Vermaak I, Viljoen A. A comprehensive scientific overview of Garcinia cambogia. Fitoterapia. 2015; 102:134–48.
2. Crescioli G, Lombardi N, Bettiol A, Marconi E, Risaliti F, Bertoni M, et al. Acute liver injury following Garcinia cambogia weight-loss supplementation: case series and literature review. Intern Emerg Med. 2018;13(6):857-72.
3. Actis GC, Bugianesi E, Ottobrelli A, Rizzetto M. Fatal liver failure following food supplements during chronic treatment with montelukast. Digestive Liv Dis. 2007; 39:953–5.
4. Chen GC, Ramanathan VS, Law D, Funchain P, Chen GC, French S et al. Acute liver injury induced by weight-loss herbal supplements. World J Hepatol. 2010; 2:410–5.
5. Corey R, Werner KT, Singer A, Moss A, Smith M, Noelting J et at. Acute liver failure associated with Garcinia cambogia use. Ann Hepatol. 2016; 15:123–6.
6. Dara L, Hewett J, Lim JK. Hydroxycut hepatotoxicity: a case series and review of liver toxicity from herbal weight loss supplements. World J Gastroenterol.2008; 14:6999–7004.
7. Elinav E, Pinsker G, Safadi R, Pappo O, Bromberg M, Anis E et al. Association between consumption of Herbalife nutritional supplements and acute hepatotoxicity. J Hepatol. 2007; 47:514–20.
8. Fong TL, Klontz KC, Canas-Coto A, Casper SJ, Durazo FA, Davern TJ 2nd et al. Hepatotoxicity due to hydroxycut: a case series. Am J Gastroenterol. 2010; 105:1561–6.
9. Jones FJ, Andrews AH. Acute liver injury associated with the herbal supplement hydroxycut in a soldier deployed to Iraq. Am J Gastroenterol. 2007; 102:2357–8.
10. Kothadia JPRR, Olivera-Martinez M. Hepatoxicity associated with Garcinia cambogia used as a weight loss supplement. Am J Gastroenterol. 2016; 111:S881.
11. Lunsford KE, Bodzin AS, Reino DC, Wang HL, Busuttil RW. Dangerous dietary supplements: Garcinia cambogia-associated hepatic failure requiring transplantation. World J Gastroenterol. 2016;22:10071–6.
12. McDonnell WM, Bhattacharya R, Halldorson JB. Fulminant hepatic failure after use of the herbal weight-loss supplement exilis. Ann Intern Med. 2009; 151:673–4.
13. Melendez-Rosado J, Snipelisky D, Matcha G, Stancampiano F. Acute hepatitis induced by pure Garcinia cambogia. J Clin Gastroenterol. 2015; 49:449–50.
14. Schoepfer AM, Engel A, Fattinger K, Marbet UA, Criblez D, Reichen J et al. Herbal does not mean innocuous: ten cases of severe hepatotoxicity associated with dietary supplements from Herbalife products. 2007; J Hepatol 47:521–6.
15. Shim M, Saab S. Severe hepatotoxicity due to Hydroxycut: a case report. Dig Dis Sci. 2009; 54:406–8.
16. Smith RJ, Bertilone C, Robertson AG. Fulminant liver failure and transplantation after use of dietary supplements. Med J Aust. 2016; 204:30–2.
17. Stevens T, Qadri A, Zein NN. Two patients with acute liver injury associated with use of the herbal weight-loss supplement hydroxycut. Ann Intern Med. 2005; 142:477–8.
18. Stickel F, Droz S, Patsenker E, Bogli-Stuber K, Aebi B, Leib SL. Severe hepatotoxicity following ingestion of Herbalife nutritional supplements contaminated with Bacillus subtilis. J Hepatol. 2009; 50:111–7.
19. Vitalone A, Menniti-Ippolito F, Moro PA, Firenzuoli F, Raschetti R, Mazzanti G. Suspected adverse reactions associated with herbal products used for weight loss: a case series reported to the Italian national institute of health. Eur J Clin Pharmacol 67:215–24.
20. Cotovio G, Oliveira-Maia AJ. Hypomania induced by a Garcinia cambogia supplement. Aust N Z J Psychiatry. 2017;51:641–2.
21. Narasimha A, Shetty PH, Nanjundaswamy MH, Viswanath B, Bada Math S (2013) Hydroxycut—dietary supplements for weight loss: can they induce mania? Aust N Z J Psychiatry 47:1205–6.
22. Nguyen DC, Timmer TK, Davison BC, McGrane IR. Possible Garcinia cambogia-induced mania with psychosis: a case report. J Pharm Pract. 2017; 1:897190017734728.
23. Wong MK, Darvishzadeh A, Maler NA, Bota RG. Five supplements and multiple psychotic symptoms: a case report. Prim Care Companion CNS Disord. 2016.
24. Hendrickson BP, Shaikh N, Occhiogrosso M, Penzner JB. Mania induced by Garcinia cambogia: a case series. Prim Care Companion CNS Disord. 2016.
25. Allen SF, Godley RW, Evron JM, Heider A, Nicklas JM, Thomas MP. Acute necrotizing eosinophilic myocarditis in a patient taking Garcinia cambogia extract successfully treated with highdose corticosteroids. 2014; Can J Cardiol 30(1732):e13–e15.
26. Joseph DJM, Levine M. Stress induced cardiomyopathy after ingestion of Garcinia cambogia. Clin Toxicol. 2014; 52:739–40.
27. Lopez AM, Kornegay J, Hendrickson RG. Serotonin toxicity associated with Garcinia cambogia over-the-counter supplement. 2014; J Med Toxicol 10:399–401.
28. Roche B, Chenoweth JA, Radke JB, Poppenga RH, Sutter ME. Hypoglycemia associated with Garcinia Cambogia ingestion. 2014; Clin Toxicol 52:736.
29. Sikka G, Gupta A, Bachan M, Khan Z. “Uber-trim” causes immune thrombocytopenic purpura: a life threatening case report. 2016; Chest 150:392A.
30. Dehoney S, Wellein M. Rhabdomyolysis associated with the nutritional supplement Hydroxycut. Am J Health Syst Pharm. 2009;66:142–8.
31. Hines EQDTE, Melville LD, Su MK. Severe rhabdomyolysis associated with Garcinia cambogia. Clin Toxicol. 2015; 53:746–7.
32. Mansi IA, Huang J. Rhabdomyolysis in response to weightloss herbal medicine. Am J Med Sci. 2004: 327:356–7.
33. Bystrak T, Cervera-Hernandez ME, Reddy N, King Z, Bratberg J. Garcinia Cambogia, diabetic ketoacidosis, and pancreatitis. 2017; R I Med J 100:48–50.
34. Sidhu RLS, Khehra L. Garcinia cambogia: a link between the “miracle” weight loss pill and acute pancreatitis. Am J Gastroenterol. 2016; 111:S560–S1.
35. Dietz B, Bolton JL Botanical dietary supplements gone bad. Chem Res Toxicol 2007: 20:586–90.
36. Bhat SP, Sharma A. Current Drug Targets in Obesity Pharmacotherapy - A Review. Curr Drug Targets. 2017;18(8):983-93.
37. Pajor EM, Oenema A, Eggers SM, de Vries H. Exploring beliefs about dietary supplement use: focus group discussions with Dutch adults. Public Health Nutr 2017; 20:2694–705.


